Application Note SpectraMax M5マルチモードマイクロプレートリーダーでの
IMAP FPキナーゼアッセイ
- 均質なFPアッセイはHTSに適したフォーマットを提供
- ロバストなZ'ファクター値による正確で再現性の高いデータ
- SoftMax Proソフトウェアで設定済みのプロトコル
PDF版(英語)
プロテインキナーゼは、多くの細胞内プロセスの制御において中心的な役割を担っている。近年、キナーゼはがんやその他多くの疾患に対する最も重要な創薬標的のひとつに浮上している。Molecular Devices社のIMAP® テクノロジーは、幅広いキナーゼの迅速な非放射性アッセイを可能にし、アッセイ開発とハイスループットスクリーニングの両方に適しています。IMAPテクノロジーは、ナノ粒子上に固定化された金属配位錯体を介したリン酸の結合に基づいている。IMAP結合体がキナーゼ反応によって生成したリン酸化ペプチドに結合すると、ペプチドの分子運動が変化し、ペプチドに結合した蛍光ラベルの蛍光偏光が増加する(図1)。このホモジニアスなアッセイは簡便で、ペプチド基質の配列に関係なく多くのキナーゼに適用できる。
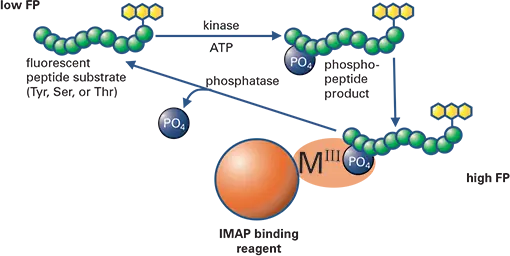
図1. IMAP FPアッセイの原理。IMAP FPキナーゼアッセイ原理図
SpectraMax® M5マルチモードマイクロプレートリーダーは、IMAPアッセイを用いたアッセイ開発やハイスループットスクリーニングに最適です。このモノクロメーターベースの装置では、追加のフィルターセットを購入することなく、選択した蛍光色素に最適な波長を選択することができます。このアプリケーションノートでは、SpectraMax M5 マイクロプレートリーダーと SoftMax® Pro ソフトウェアを使用して、緑色および赤色標識蛍光基質を用いた IMAP 蛍光偏光(FP)キナーゼアッセイと検量線を実行する方法について説明します。酵素希釈曲線は、T細胞シグナル伝達に重要な役割を果たすチロシンキナーゼであるLckと、ホスファチジルイノシトール3キナーゼシグナル伝達と細胞生存に関与するセリン-スレオニンキナーゼであるAkt1/ PKBαについて行った。スタウロスポリンによるAkt1/PKBαの阻害もアッセイした。FAMおよびTAMRA標識ペプチド基質の両方で高いZ'ファクター値が得られ、フィルターベースのAnalyst® HT Multi-Mode Microplate Readerで得られたデータと同等の結果が得られた。
材料
- プログレッシブ結合システム付きIMAP Screening Expressキット(Molecular Devices Cat.)
◦IMAPプログレッシブ結合試薬
◦IMAP Progressive Binding Buffer A(5X)
◦IMAP Progressive Binding Buffer B(5X)
◦IMAP Reaction Buffer(5X)
- Lckキナーゼ(Upstate Cat. #R7159)
◦FAM-p34cdc2由来ペプチド(Molecular Devices社製 Cat.)
◦TAMRA-p34cdc2 由来ペプチド(Molecular Devices 社製 Cat.)
◦FAM-p34cdc2 由来リン酸化ペプチドキャリブレーター(Molecular Devices 社製 Cat.)
- Akt1-PKBαキナーゼ (Upstate Cat. #14-276)
◦FAM-Crosstide(モレキュラーデバイス社製 Cat.)
◦FAM-ホスホ-Crosstide(モレキュラーデバイス社製 Cat.)
-
アデノシン5'三リン酸(ATP)、精製水中50 mMストック(Sigma Cat.)
-
DL-ジチオスレイトール(DTT)、精製水中100mMストック(Sigma Cat.)
-
スタウロスポリン(Biomol Cat.)
-
黒色384ウェルポリスチレンマイクロプレート(Corning Cat.)
-
SpectraMax M5マルチモードマイクロプレートリーダーとSoftMax Proソフトウェア(Molecular Devices社製)
方法
キナーゼ反応
ステップ1: 1X IMAP Reaction Bufferに最終濃度1mMのDTTを加えてComplete Reaction Buffer(CRB)を調製する(100mM DTTストックの1:100希釈)。
ステップ2: FAMor TAMRA標識ペプチド基質の400 nM(4X)ストックをCRBで調製する(20 µMペプチドストックの1:50希釈)。
ステップ3: ATPの20 µM(4X)ストックをCRBで調製する(50 mM ATPストックの1:2500希釈)。
ステップ4:アッセイに必要な4倍濃度の酵素希釈系列を調製する。キナーゼ阻害アッセイには、一定濃度の酵素を使用し、スタウロスポリンまたは他のキナーゼ阻害剤の希釈系列を作成する。希釈にはCRBを使用する。
ステップ5:酵素アッセイウエルに以下のものをピペッティングして、キナーゼ反応をセットアップする:
- 5 µL CRB またはスタウロスポリン
- 5 µL 酵素(酵素バックグラウンドのないサンプルの場合は、5 µL CRB で代用する)
- 20-µM ATPストック 5 µL
- 400-nM ペプチドストック 5 mL
ステップ6:室温で1~1.5時間インキュベートする。
注:より詳細な手順については、IMAP 製品添付文書を参照してください。
キャリブレーションスタンダード
ステップ1: CRBに100-nMのペプチドストックを調製する(キナーゼアッセイと同じペプチド基質を使用する)。
ステップ2: CRBで100-nMリン酸化ペプチドストックを調製する(キナーゼアッセイで使用した基質のリン酸化バージョンを使用する)。
ステップ3:ペプチドとリン酸化ペプチドのストックを合わせて、表1に示すキャリブレーション用スタンダードとする。表1に示す量は、四重反復サンプルを調製するのに十分な量である。
|
キャリブレーションスタンダード (リン酸化率) |
µL ペプチド ストック |
µL リン酸化ペプチド
ストック |
|---|---|---|
| 0 | 100 | 0 |
| 12.5 | 87.5 | 12.5 |
| 25 | 75 | 25 |
| 50 | 50 | 50 |
| 100 | 0 | 100 |
表1. 検量線標準液の調製
ステップ 4: 20 µL CRB を含む緩衝液のみのバックグラウンド検体を含め、各キャリブレーショ ン標準物質を 20 µL ずつ 4 重ウエルに分注します。
結合反応
ステップ 1: 75% Progressive Binding Buffer A と 25% Progressive Binding Buffer B を混合し、Progressive Binding Buffer を調製します。
ステップ 2: Progressive Binding Buffer で Progressive Binding Reagent を 1:600 に希釈し、Binding Solution を調製します。
ステップ3:各アッセイウェルおよびキャリブレーションスタンダードウェル(バッファバックグラウンドサンプルを含む)に60μLの結合溶液をピペッティングします。
ステップ4:遮光し、室温で1時間インキュベートします。
SoftMax Proでテンプレートをセットアップし、SpectraMax M5マイクロプレートリーダーでプレートを読み取ります:
注:FAMおよびTAMRA標識基質で使用するIMAP FPプロトコルは、SoftMax Pro 5のBinding Assaysプロトコルフォルダーにあります。
ステップ1:使用する蛍光色素に特化したSoftMax Pro IMAP FPプロトコルを開きます。FAMまたはTAMRA以外のフルオロフォアを使用する場合は、波長設定を調整してください。SpectraMax M5マイクロプレートリーダーの設定を表2に示す。
| 読み取りタイプ | エンドポイント | ||||||||||
| 読み取りモード | 蛍光偏光 | ||||||||||
| 波長 |
|
||||||||||
| 感度 |
読み取り 100 PMT: 高または中 |
||||||||||
| オートミックス | オフ | ||||||||||
| オートキャリブレーション | オン | ||||||||||
| アッセイプレートタイプ | 384ウェル Costar black | ||||||||||
| 読み取るウェル数 | [ユーザーにより決定される] | ||||||||||
| セットリング時間 | 100 ms | ||||||||||
| 自動読み取り | オフ | ||||||||||
表 2. SpectraMax M5マイクロプレートリーダー用SoftMax ProのIMAP FP設定
ステップ2:バックグラウンド検体、キナーゼアッセイ検体、キャリブレーション標準物質を指定する実験テ ンプレートをセットアップする。キナーゼアッセイサンプルとキャリブレーション標準液は、SoftMax Proテンプレート内の8つの設定済み'Sample'グループに割り当てることができます。バッファーのみのコントロールを対応する'Background'グループに割り当てることで、ミリ偏光(mP)値を計算する前にバックグラウンド蛍光を自動的に差し引くことができます。
ステップ3:マイクロプレートをプレートリーダーキャリッジにセットし、Readをクリックします。
結果
SoftMax Pro IMAP FPプロトコルは、平行および垂直の平均値、mP、全強度、標準偏差、CVを自動的に計算します。各アッセイサンプルセットのグループテーブルでは、テンプレートで指定されたバックグラウンドサンプルをリファレンスとして、バックグラウンド減算mPが計算されます。リン酸化率は、適切な検量線から外挿することによっても算出できる。
図2は、FAM-p34cdc2由来ペプチドを用いて得られたLckキナーゼ希釈曲線を示す。このプレートを SpectraMax M5 マイクロプレートリーダーで読み取ると、酵素濃度範囲 0.04~3.5 unit/mL でデルタ mP は 303、Z'ファクターは 0.87 であった2。 図 3 は、同じアッセイプレートを Analyst HT マルチモードリーダーで読み取ったものである。デルタmPは336で、Z'ファクターは0.95であった。どちらの装置でもEC50は0.5 unit/mLであった。
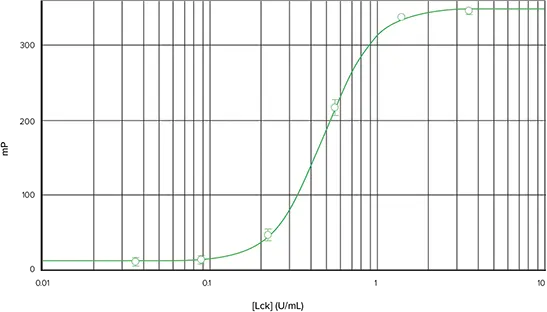
図2. SpectraMax M5マイクロプレートリーダーを用いたIMAP FPキナーゼアッセイ。SpectraMax M5で読み取った、0.04から3.5単位/mLの酵素にFAM-p34cdc2由来ペプチドを加えたLckキナーゼ希釈曲線(4パラメータ曲線フィット)。エラーバーは標準偏差。
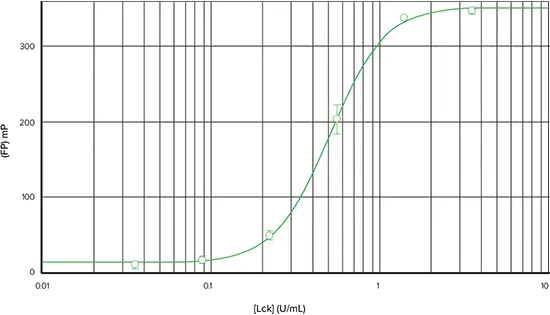
図3. Analyst HTを用いたIMAP FPキナーゼアッセイ。Analyst HTで読み取ったFAM-p34cdc2由来ペプチドによるLckキナーゼ希釈曲線(0.04~3.5ユニット/mL酵素)(4パラメータ曲線フィット)。
非リン酸化ペプチド対照とリン酸化ペプチド対照を用いて別々の検量線を設定すれば、mPの値をリン酸化パーセンテージに変換することができます(図4)。まず新しいグラフを作成し('Graph#1'がソフトウェアによって割り当てられたデフォルトの名前です)、キャリブレーターサンプルグループのmP対リン酸化パーセント(濃度)をプロットします。このプロットのデフォルト名は 'Plot#1' です。検量線標準物質グループの表に、以下の式で新しい列を挿入します: InterpX('Plot#1@Graph#1@IMAP FP_FAM',AvgbkgsubmP)。'IMAP FP_FAM' は実験タイトルである。
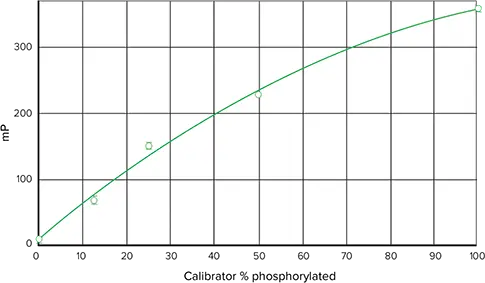
図4. FAM標識ペプチドを用いたIMAP。SpectraMax M5で読み取ったFAM-p34cdc2由来ペプチドとリン酸化ペプチドによる検量線標準曲線(二次曲線フィット)。
赤色蛍光体を用いたIMAPキナーゼアッセイの性能を決定するために、TAMRA-p34cdc2-由来ペプチドを用いて別のLckキナーゼ希釈曲線を行った(図5)。SpectraMax M5マイクロプレートリーダーで読み取ると、酵素濃度範囲0.04~3.5 unit/mLで、Z'ファクター0.95、デルタmP258が得られた。図6では、同じアッセイプレートをAnalyst HTリーダーで読み取 り、デルタmPは270、Z'ファクターは0.93であった。どちらの装置でもEC50は0.4 unit/mLで、FAM標識基質によるEC50に近い値であった。対応する検量線も設定された(図7)。両装置でTAMRA標識ペプチド基質を用いた結果とFAM標識基質を用いた結果が類似していることから、ユーザーは、被験化合物から放出されるバックグラウンド蛍光を最小限に抑えるなど、赤色標識蛍光色素の利点を活用することができる。
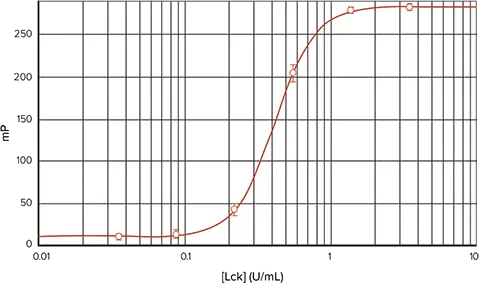
図5. SpectraMax M5マイクロプレートリーダーを用いたTAMRA標識ペプチドによるLckキナーゼアッセイ。SpectraMax M5で読み取ったTAMRA-p34cdc2由来ペプチドによるLckキナーゼ希釈曲線(4パラメータ曲線フィット)。
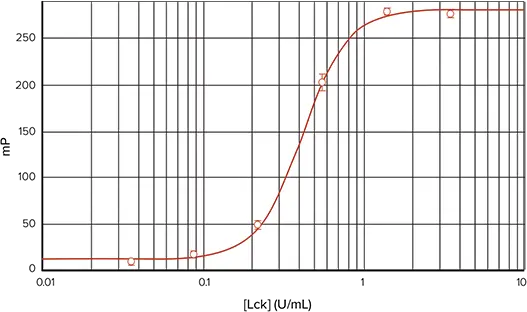
図6. Analyst HT を用いた TAMRA 標識ペプチドによる Lck キナーゼアッセイ。Analyst HTで読み取ったTAMRA-p34cdc2由来ペプチドによるLckキナーゼ希釈曲線(4パラメータ曲線フィット)。
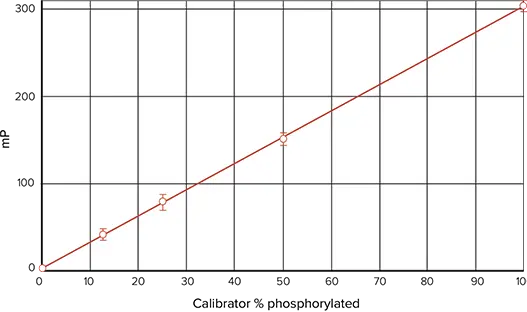
図7. TAMRA標識ペプチドを用いたIMAP。SpectraMax M5 で読み取った TAMRA-p34cdc2 由来ペプチドとリン酸化ペプチドによる検量線標準曲線(直線曲線フィット)。
別のキナーゼを用いた SpectraMax M5 マイクロプレートリーダーでの IMAP FP アッセイの性能を示すために、基質として FAM-Crosstide を用いて Akt1/PKBα の酵素希釈曲線を得た。図8では、0.002~5.4 units/mLの酵素濃度範囲で、339のデルタmPと0.92のZ'ファクターが得られた。スタウロスポリンによるAkt1/PKBαの阻害を図9に示す;ここでのデルタmPは199で、Z'ファクターは0.93であった。このアッセイに対するスタウロスポリンのIC50の計算値は19.7nMであった。ここでは酵素希釈曲線よりもデルタmPが低かったが、これは阻害アッセイに約75%の最大リン酸化を与えるキナーゼ濃度が選ばれたためである。
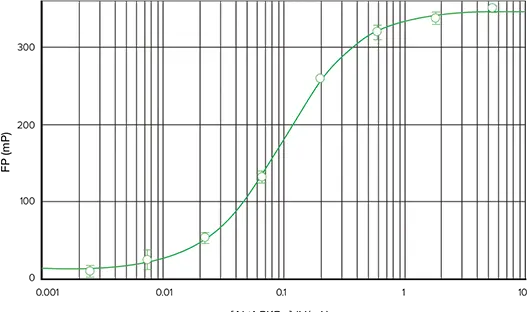
図8. SpectraMax M5マイクロプレートリーダーを用いたFAM標識ペプチドによるAkt/PBKaキナーゼアッセイ。SpectraMax M5で読み取ったFAM-Crosstide基質を用いたAkt1/PKBαキナーゼ希釈曲線(4パラメータ曲線フィット)。
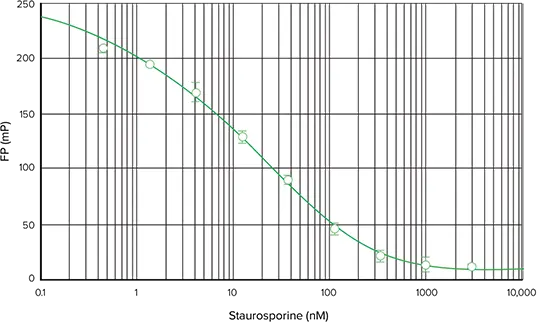
図9. SpectraMax M5マイクロプレートリーダーでのキナーゼ阻害。SpectraMax M5で読み取った、スタウロスポリンとFAM-Crosstide基質を用いたAkt1/PKBαキナーゼ阻害曲線。ここでは、SoftMax Pro 5で利用可能な5パラメータ曲線フィットを使用した。
結論
細胞シグナル伝達や疾患におけるキナーゼの役割を理解し、治療薬となりうるキナーゼモジュレーターを同定しようとする研究者は、アッセイ開発とハイスループットスクリーニングの両方に適した非放射性のホモジニアスアッセイにますます注目している。ホモジニアスFPアッセイは、キナーゼ活性化因子、阻害剤、基質を同定するためのHTSに適したフォーマットを提供する。SpectraMax M5 マイクロプレートリーダーで IMAP FP キナーゼアッセイを実行すると、正確で再現性のあるデータが得られ、Z'ファクター値も堅牢です。デュアルモノクロメーターシステムにより、追加のフィルターセットを購入することなく、幅広い蛍光標識ペプチド基質を用いてアッセイを最適化することができる。緑または赤で標識された基質を用いたIMAP FPキナーゼアッセイの結果は、フィルターベースのAnalystマイクロプレートリーダーで得られた結果と非常によく似ている。SoftMax Pro 5のIMAP FPプロトコールは、FPデータの取得と計算を行う便利な方法を提供し、あらゆる蛍光色素に簡単に適応できます。
参考文献
- IMAP Akt Assay Kit Product Insert(Molecular Devices製品番号R8058)
- Zhang, J.H., Chung, T.D.Y., and Oldenburg, K.R. (1999). ハイスループットなスクリーニングアッセイの評価とバリデーションに使用する簡単な統計パラメータ。J Biomol Screen 4(2): 67-73.
PDF版(英語)