2023/2/10
アッセイ準備の整った患者由来オルガノイド(PDO)と
ハイスループット3Dイメージングによる創薬の進展事例
はじめに-問題
ロンドン・スクール・オブ・エコノミクスが2020年3月に実施した調査(www.lse.ac.uk)によると、新薬の臨床導入にかかる平均コストは約10億ドルである。これは、創薬の初期段階でスクリーニングに使用される代表的なモデルが不十分で、医薬品開発パイプラインの後半で化合物の高い失敗率につながっていることが一因である。このため、さらなる臨床開発のためのリード候補を早期に正確に選択するため、より患者中心のモデルが求められている。
患者由来オルガノイド(PDOあるいは単に "オルガノイド "と呼ばれる)は、三次元的に培養され、この問題に対する解決策となる。PDOは、その元となる正常組織や疾患組織のミニチュアコピーであり、人体の3次元組織を完全に表現している。その証拠に、患者とその由来のオルガノイドを同じ薬剤で治療すると、鏡像反応を示すことが示されている(Vlachogiannis et al.) このことは、オルガノイドが潜在的治療薬の「ライブラリー」のスクリーニングに使用できるという原理を証明している。患者オルガノイドに望ましい効果をもたらす化合物は、患者自身の治療にも有効である可能性が高い。
患者由来オルガノイド(PDO)とは?
- 正常または疾患患者の生検組織由来
- タンパク質ゲル中で3次元的に成長させ、液体を供給する
- 複数のセルタイプから形成される(体内の臓器と同様)
- ミニチュア臓器の複製(例:「ミニ内蔵」)。
- ヒト生物製剤を完全に再現
- 創薬に使用する特許取得済み「アバター
- バイオプロセッサーで培養し、1バッチあたり数百万個の標準化されたコピーを作成
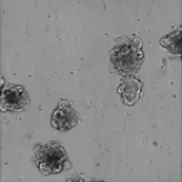
3D大腸がん患者由来オルガノイド(PDO)の明視野画像
理想的には、薬剤が適切にテストされ、臨床での使用が許可されれば、患者自身のオルガノイドの反応に基づいて、個々の患者に個別の薬剤治療がデザインされるだろう。残念なことに、オルガノイドを作製・拡大するには、現在のところ実験室で数週間を要する。臨床医は、治療を開始するまでにそれほど長く待ちたくないだろう。将来、オルガノイドの誘導、培養、拡大技術がさらに洗練され、開発されれば、個別化治療が可能になるかもしれない。
3Dオルガノイドは比較的新しい技術であり、それをフルに活用するためのアッセイはまだ発明・開発されていない。研究者たちは、より複雑ではないが、ヒトの生物学を正確に表現していない2次元細胞単層での研究に慣れている。
その課題とは、初期スクリーニングから化合物を正確に選択し、さらなる開発や臨床試験につなげることである。
生存率アッセイは、化合物の有効性(「有効性」)を定量化するための一般的な方法の一つである。よく使われる手法の一つに、ATPレベルを測定することで代謝的に活性な細胞の存在を検出する生物発光ベースのアッセイがある。ハイコンテントイメージャーは、未処理のコントロール(および場合によっては非がん組織由来のオルガノイド)と比較して、薬剤を投与したサンプルの生細胞または死細胞(一般的な生細胞マーカーであるカルセインAMなどの色素で標識)の数をカウントすることにより、細胞の生存率を測定するためにも使用できる。治療で使用される薬剤の望ましい効果は、健康な組織には影響を与えずに、できるだけ多くのがん細胞を死滅させることである。特に高濃度の治療薬が使用される場合、未処置のサンプルでまだ生きている細胞の数は、薬物処理された細胞よりもかなり多くなる。したがって、2つの条件の違いを定量化し、トラメチニブのような抗癌剤が有効かどうかを判断することが重要である。同じ原理で、化合物のライブラリーからスクリーニングの一環として、がん細胞を殺すのに効果的に働く新しい治療薬を同定することができる。
すべての薬が同じように作用するわけではない。一部の薬剤は、オンターゲットされた細胞のサブセットに特異的に作用したり、細胞内のシグナルを変化させたりして、病気の再発や拡大を防ぐ。細胞を大量に殺す効果はないので、健康な細胞とがん細胞の違いは、治療後に残っている生きた細胞の数を数えることによって簡単に区別したり定量したりすることはできない。別の方法論が必要である。
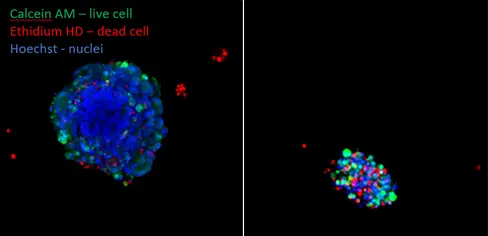
大腸癌オルガノイドを未処理のまま(A)、またはトラメチニブ(5mM)に曝露した(B)。生きた細胞(緑、カルセインAM)と死んだ細胞(赤、エチジウムホモダイマー)を示すために、5日後に染色した。トラメチニブ処理後、生きた細胞はほとんど残っていないことがはっきりとわかる。
解決策 - ハイスループット3Dイメージングにより、特異性に作用する薬物の微妙な効果を検出する。
科学者たちは、オルガノイドを薬剤で処理すると、細胞に対する薬剤の効果に関連した外観(形態)の顕著な変化が生じることを観察してきた。細胞生存能に加えて、細胞骨格構造、ミトコンドリア、オルガノイド全体の形態など、細胞やオルガネラに特異的な情報を得るために、他の蛍光マーカーをサンプルに加えることができる。ハイコンテントイメージャーでオルガノイドの画像を撮影し、データ解析ツールを使って変化を定量化することで、未知の化合物が効果を発揮する時期を示すことができる可能性がある。これは、生細胞/死細胞アッセイで処理細胞と未処理細胞の違いを検出できない場合に特に関連する。(Badderら、2020)。
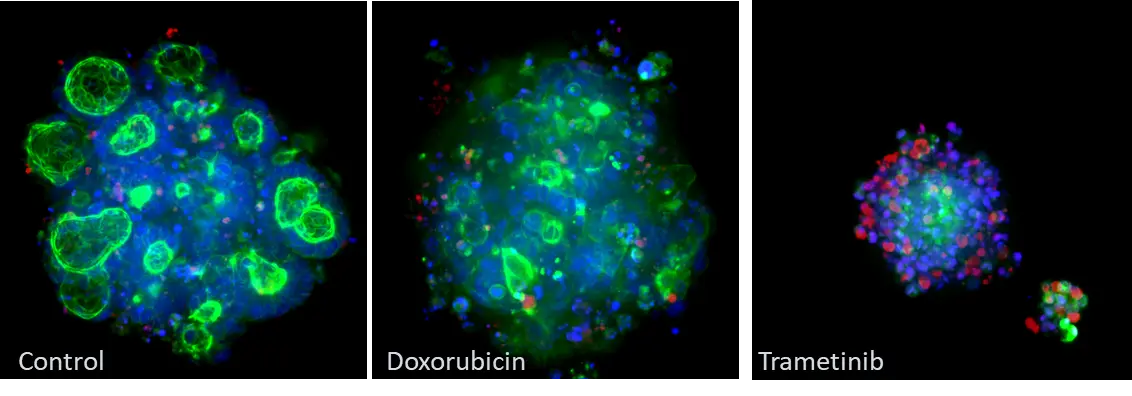
Molecular Devices社のImageXpress® Micro Confocalシステムを用いて撮影した形態変化の例。CRCオルガノイドを固定し、ファロイジン(緑)、ヘキスト(青)、エチジウムホモダイマー(赤)で染色した。コントロール群と治療群のファロイジン染色(緑色)の変化に注目。
3Dオルガノイド・イメージングが創薬に利用できるという原理をさらに実証するために、CellesceはMolecular Devicesの最先端の自動化技術、イメージング技術、3Dイメージング・データセットの高度な解析を用いて、未治療と薬剤処理した大腸がんオルガノイドの物理的特性を比較した。人工知能支援画像解析ツールを用いてCRC画像を解析し、様々な画像記述子を用いて治療の効果を定量化した。測定可能なものの一例、すなわち総面積を以下に示す。
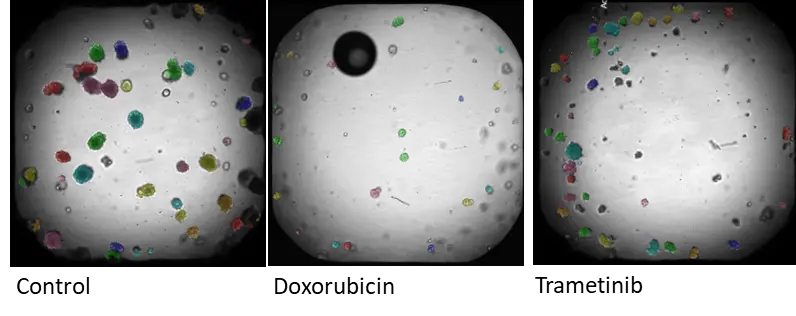
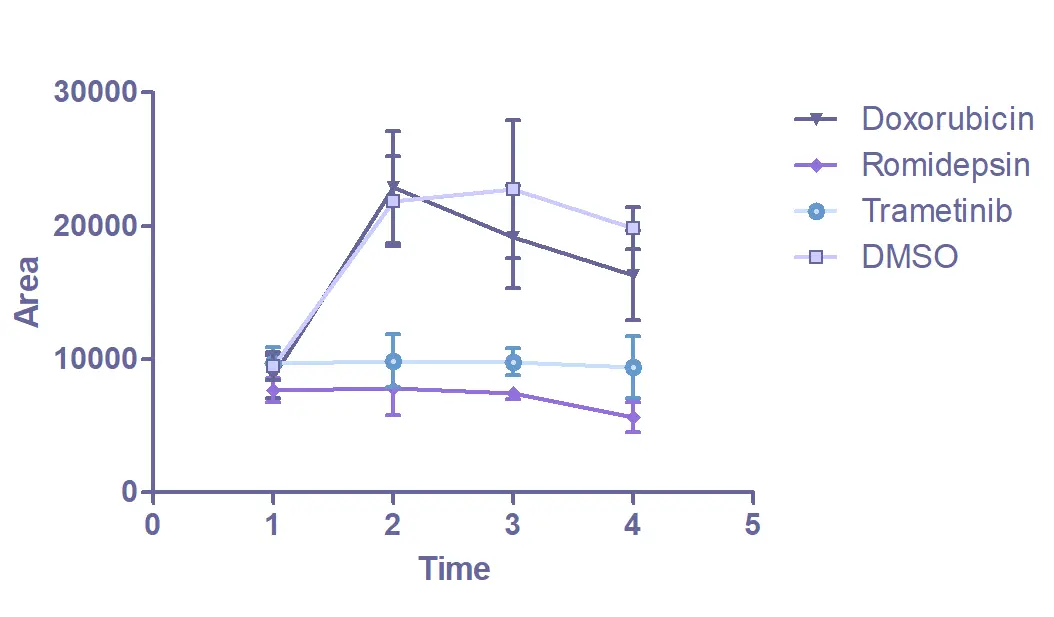
ImageXpress Confocalで撮影したオルガノイドの画像。オルガノイドの形態の経時的変化をモニターするために明視野イメージングを使用。解析はIN Carta画像解析ソフトウェアで行う。同定された各オルガノイドはカラーマスクでオーバーレイされている。グラフ(E)は、5日間の平均オルガノイド面積の変化を示す。
総面積が最も減少したのは、ロミデプシンとトラメチニブで処理したオルガノイドであった。対照と比較して、ロミデプシンとトラメチニブによる治療はオルガノイドの成長を停止させた。この結果は生存能アッセイのデータと一致しており、ロミデプシンおよびトラメチニブで処理したオルガノイドは未処理のコントロールと比較して死細胞の有意な増加(細胞総数に占める割合)を示した。イメージングデータの初期解析により、オルガノイドの形態と薬物反応の関係が確認された。これによって、この手法が薬剤スクリーニングに使えることが証明された。
オルガノイドと3Dイメージングの利用は、創薬の初期スクリーニングに革命をもたらす可能性がある。そのためには、大量のオルガノイドの標準化された再現性のあるバッチが必要である。オルガノイドは手作業で培養されるため、この要件を満たすのは容易ではない。Cellesceは、特許取得済みのバイオプロセスの開発を通じて、このニーズに対応した。この斬新でユニークな技術は、バイオプロセッサーを使用して、ハイループットスクリーニングに十分な量のオルガノイドを制御された方法で生産するものである。モレキュラー・デバイス社は、ロボット工学を用いたサンプルハンドリングの自動化、イメージングとデータ解析を用いたアッセイの最適化という追加要件にも取り組んでいる。
アッセイ準備の整ったオルガノイドの使用は、ハイスループットスクリーニングと定量アッセイの自動化とともに、大規模化合物ライブラリーからの候補治療薬の正確な選択を促進する。これは、効果的な治療法を特定し、創薬パイプラインを加速させるプロセスに向けて、大いに役立つだろう。創薬の初期段階で治療薬候補化合物を正確に選択することは、資源の浪費と開発コストの削減につながる。その結果、上市される薬剤の数が増えることになる。こうして臨床医は、それぞれの患者に最も適した、副作用の少ない治療法を選択できるようになる。これにより、生活の質が改善され、生存率が向上する。
医薬品開発の改善 モレキュラー・デバイセズとCellesceはオルガノイドの利用促進を目指す
今回のCellesce社の買収は、創薬プロセスを転換し、新規治療薬の開発を促進する3Dバイオロジー技術への投資に対するモレキュラー・デバイセズのコミットメントを確認するものです。
「CellesceのCEOであるVicky Marsh-Durban氏は、「モレキュラー・デバイスは、Cellesceの技術をさらに発展させ、その可能性を最大限に活用するための能力、評判、リーチ、リソースを有しています。「Cellesceの専門知識と知的財産をモレキュラー・デバイスに提供することで、創薬研究に革命をもたらし、ヒトに関連する3Dバイオロジー研究の可能性を最大限に引き出すことができるのです。
インストゥルメント・ビジネス・アウトルックのターニャ・サマザンとモレキュラー・デバイスのスーザン・マーフィー社長、Cellesceのヴィッキー・マーシュ=ダーバンCEOとの対談をさらに詳しくご覧ください。
オルガノイドeBookのダウンロード
創薬研究におけるオルガノイドの歴史、現在の役割、将来的な影響、そしてオルガノイドを研究にうまく取り入れる方法について詳しく解説しています。