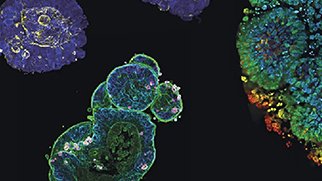
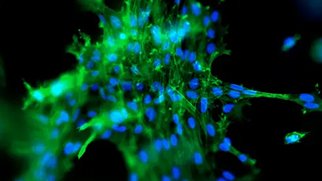
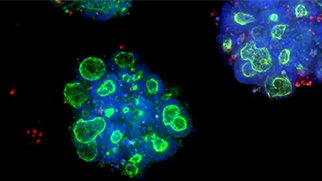
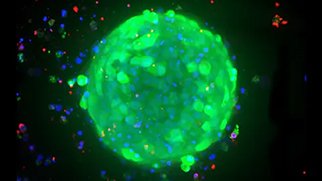
疾患モデリングとは何か?
疾患モデリングは生物医学研究の基本的な側面であり、制御された環境において疾患の挙動を模倣する代表的なシステムの作成を包含します。これらのモデルは、研究者が疾患の根底にあるメカニズムについて洞察を深め、潜在的な治療法の有効性を検証し、最終的には患者ケアの改善に道を開くのに役立っています。
疾患モデルシステムの範囲は、単純な2D細胞培養から複雑なモデル生物まで、その複雑さと規模は多岐にわたります。モデル生物はin vivoの環境を提供しますが、コストがかかることが多く、ヒューマンバイオロジーでは表現できないことがあります。一方、従来の2D細胞培養システムは長年使用されてきましたが、生体組織に見られる複雑な3D構造や細胞間相互作用を表現するには限界がありました。その結果、3D細胞培養は、疾患モデリングのための魅力的なモデルシステムとして出現してきました。
ヒト疾患研究のための3D細胞モデルの活用
3D細胞モデルは、生体内の組織や臓器の複雑さの主要な側面を要約しており、ヒト疾患の研究に適しています。モデル生物よりも実験的に扱いやすいことに加え、3Dモデルはヒト細胞から誘導できるため、研究対象のヒト疾患との関連性が高いです。例えば、iPS細胞から培養した3D脳オルガノイドは、アルツハイマー病やパーキンソン病などの神経変性疾患の研究に、心臓オルガノイドや心臓オルガノイドは、心不全などの心血管系疾患の研究に、腫瘍生検から作製した患者由来オルガノイド(PDO)は、患者の特異的な薬物反応が分かり、より効果的な治療法を提供するための腫瘍学研究のモデルとして利用できます。
疾患研究と創薬研究のための患者由来オルガノイド
多くのがん治療薬は、in vitroではその有効性を示す有望なデータが得られているにもかかわらず、医薬品開発パイプラインの後期段階や臨床試験では失敗に終わっています。この高い失敗率の一因は、創薬の初期段階で薬剤候補のスクリーニングに使用される予測モデルの欠如にあります。そのため、新しい治療ターゲットを発見するための効率的な化合物試験に適した、より代表的なモデルを開発し利用する必要があります。
3D細胞モデル、特に患者由来オルガノイド(PDO)は、この問題に対する有望な解決策を提供します。3Dで培養された細胞は、細胞間相互作用や、がん幹細胞ニッチを含む組織微小環境をよりよく模倣することができます。研究によれば、患者とその由来のオルガノイドは薬物に対して同様の反応をすることが示されており、治療成績を向上させるためにPDOを用いることの治療的価値が示唆されています。しかしながら、アッセイの再現性、スケーラビリティ、コストなどの課題により、PDOの創薬パイプラインでの利用は制限されています。
ここでは、我々の注目すべき患者由来がんオルガノイド研究を紹介します。我々の結果は、ハイコンテントイメージングとAIデータ解析による自動化を用いた場合、プレシジョン・メディシンとハイスループット創薬アプリケーションの両方において、PDOが他の組織よりも優れた可能性を持つことを示しています。
乳がん患者由来の腫瘍細胞
トリプルネガティブ乳がんは、転移、再発、薬剤耐性の高い、臨床的に攻撃的な腫瘍サブタイプです。現在、この疾患に対して臨床的に承認された低分子の標的治療薬はなく、新たな治療標的を発見することの重要性が強調されています。原発性腫瘍由来モデルは、腫瘍の不均一性や形態、複雑な遺伝的・分子的組成を再現することができ、それによって薬剤開発や薬剤試験を加速することができます。本研究では、複雑な3D細胞ベースアッセイのスケールアップを可能にする画像イメージングと細胞培養法の自動化について説明します。
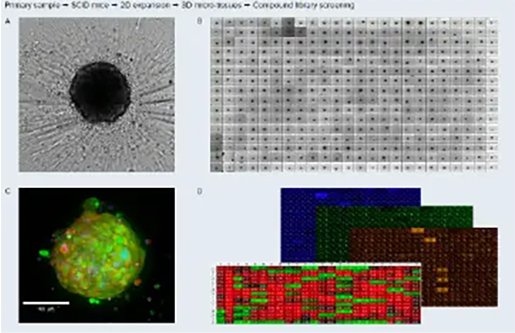
大腸がん(CRC)患者由来オルガノイド
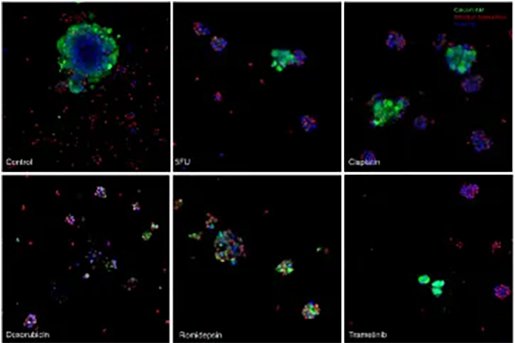
本ポスターでは、大腸がん(CRC)のPDOを用いたハイスループット・アプリケーションにおいて、その有用性を実証します。様々な濃度の抗がん剤で処理したPDOを透過光イメージングで経時的にモニターし、ディープラーニングベースの画像セグメンテーションモデルを開発して、PDOのサイズ、テクスチャー、強度、その他の形態学的および表現型の読み出しを解析しました。この結果は、化合物スクリーニングのようなハイスループットなアッセイに、アッセイ準備の整ったPDO利用の効率性をサポートするものです。
ヒトに関連する3D細胞培養モデルの種類
疾患モデリングや創薬に用いられる3D細胞モデルには、スフェロイド、オルガノイド、Organ-on-a-chipなど様々な種類があります。各タイプの3D細胞モデルにはそれぞれ独自の利点があり、どの3Dモデルを選択するかは具体的な研究内容次第です。これらのヒトに関連した3D細胞モデルを用いることで、研究者は、疾患の進行に対する様々な治療の効果を研究し、潜在的な薬剤候補を同定し、疾患メカニズムを理解できます。
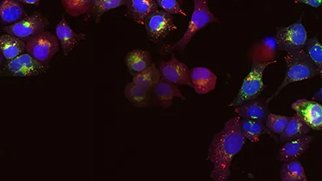
スフェロイド
スフェロイドは、特異性環境(例えば、接着性の低い表面 でコーティングされたプレーティングに播種した場合)で自己集合 する細胞の集合体です。使用されるセルタイプによって、出来上がったスフェロイドは、肝臓、乳房、膵臓組織や特異性がん組織など、様々な組織をモデル化することができます。スフェロイドは3D細胞モデルの中で最も単純なタイプで、通常は単一種類の細胞のみで構成されています。スフェロイドは増殖に時間がかからないため、作業が比較的容易です。しかし、他の3Dモデルのような構造の複雑さはありません。スフェロイドは、がん細胞や人工多能性幹細胞(iPSC)から作製することができ、がんの進行、薬剤耐性、毒性の研究に使用されます。
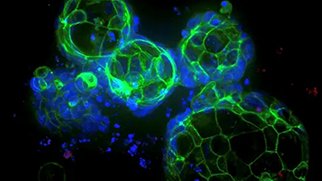
オルガノイド
3Dオルガノイドとは、脳、腎臓、腸など、特異的な臓器や組織の構造や機能を模倣した3次元構造体です。iPS細胞や成体幹細胞から作製され、疾病メカニズムの研究や様々な治療法の有効性を検証するために使用されます。ヒト組織由来であるため、疾患をよりよく再現することができます。
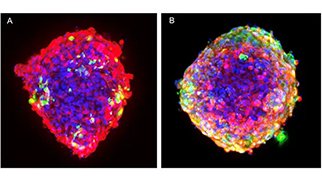
患者由来オルガノイド(または腫瘍細胞)
患者由来オルガノイド(PDO)は、健常組織と疾患組織の両方から採取した組織サンプルから培養した3D細胞構造体であり、"皿の中の患者 "を表現しています。PDOは、患者の組織に見られるセルタイプの遺伝、構造、不均一性に酷似しています。この類似性の高さと翻訳可能性の向上により、PDOは疾患研究や医薬品開発のための貴重な資源となっています。
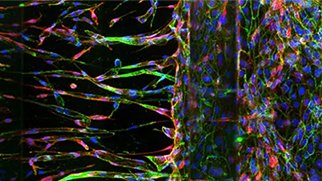
Organ-on-a-chip
これらのモデルは、マイクロ流体システムを用いて、心臓、肝臓、肺などの異なる臓器の機能を一つの装置でシミュレートするものです。病気の進行を研究したり、さまざまな薬物や治療法の有効性をテストしたりするために使用することができます。
3Dバイオプリンティング
バイオプリンティングは、3Dプリンティング技術を用いて、生きたセルと生体材料から組織や臓器などの複雑な生物学的構造を作成する比較的新しい技術です。バイオプリンティングは、研究者が複雑な生物学的システムの精密で再現可能なモデルを作成できるため、疾患モデリングの有望なツールとして浮上してきました。