2025/1/8
3Dバイオロジー: 次世代創薬のパラダイムシフト【インタラクティブ・インフォグラフィック】
原文 2023年4月19日
創薬の展望が変わりつつあります
2023年4月19日 医薬品の上市にはこれまで時間とコストがかかり、多くの候補が臨床試験の第一段階で失敗してきました。動物や2Dで増殖させた細胞培養のような従来のモデルを用いて化合物を初期段階でスクリーニングすることが、その一因である可能性を示唆する証拠が増えています。
研究者たちは現在、オルガノイドのような複雑で、ヒトに関連した3Dシステムに向かっています。
このインタラクティブなインフォグラフィックでは、業界がこの次世代の創薬を受け入れている理由や、科学者の3Dバイオロジーへの旅をサポートするイノベーションについて、詳しくご紹介しています。
PDFダウンロード
※USサイトへ遷移します
創薬パラダイムとは?
3Dバイオロジーは次世代の創薬です。2D細胞培養や動物モデルから、より生物学的な3D細胞モデルやヒトシステムへの移行です。
最新のブログでは、この新しい創薬パラダイムに参入するために必要なこと、そして世界中の研究者が化合物スクリーニングを2D細胞培養や動物モデルから、オルガノイドのようなより複雑でヒトに関連した3Dシステムへどのように移行しているかを紹介し、2Dバイオロジーから3Dバイオロジーへの旅を始めます。
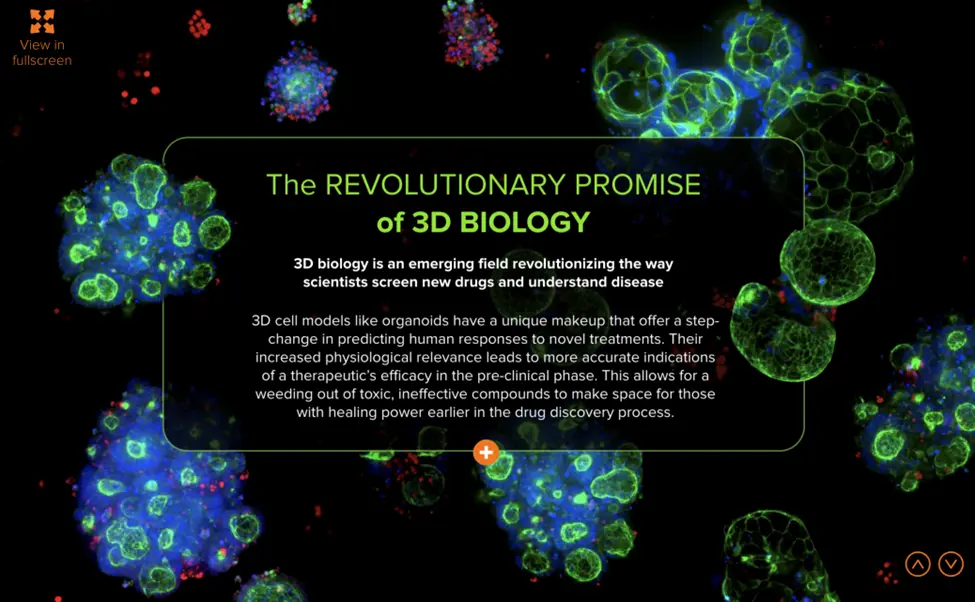
3Dバイオロジーがもたらす革命的な可能性
ヒトに関連したモデルは、ヒト細胞と薬物の相互作用に関する早期の洞察を提供し、有効性や毒性の懸念を前臨床的に検出します。3Dバイオロジーという新しい分野は、薬剤スクリーニングと疾患理解に革命をもたらし、新しい治療に対するヒトの反応を予測する上でユニークな利点を提供します。
高価で長い医薬品開発の道のり
何十億ドルもの投資が行われているにもかかわらず、新薬の承認取得には長い時間とコストがかかります。従来の2D細胞培養や動物モデルでは、ヒトでの薬効を予測できないことが多く、多くの新薬候補が開発途中で頓挫しています。
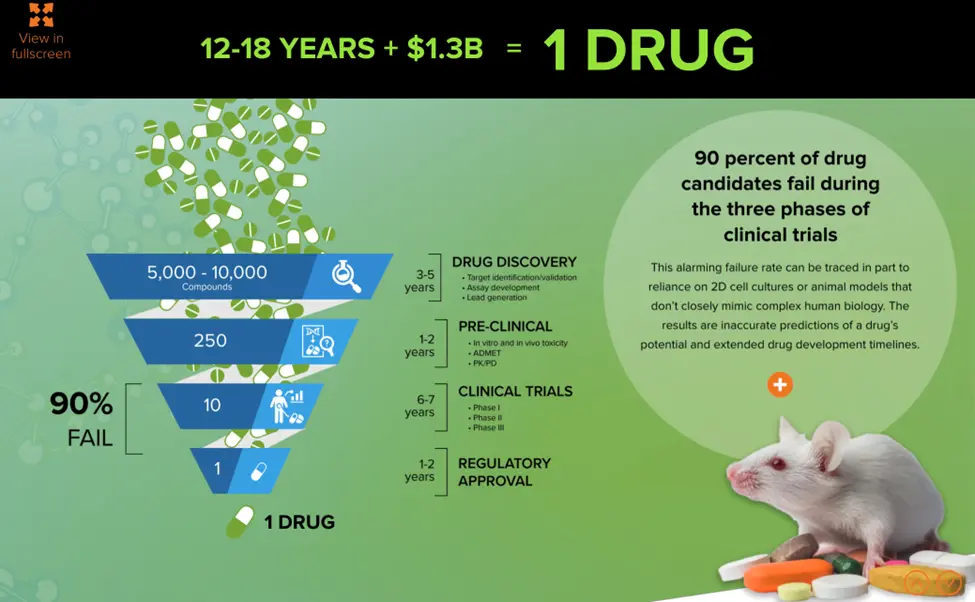
研究開発費の驚異的な75%は失敗によるもので、当初は有望と思われたプロジェクトに費やされた資金が、後にヒト試験で効果がない、安全でない、あるいは商業的に成り立たないことが判明したものです。医薬品開発プロセスに革命が必要なのは明らかであり、オルガノイドがその鍵となるかもしれません。
従来の細胞モデルの限界
倫理的配慮はさておき、2D細胞株、小動物モデル、非ヒト霊長類を問わず、医薬品研究における従来の細胞モデルは、ベンチからベッドサイドへ治療薬を移行する際の成功を妨げるトランスレータビリティの課題に直面しています。
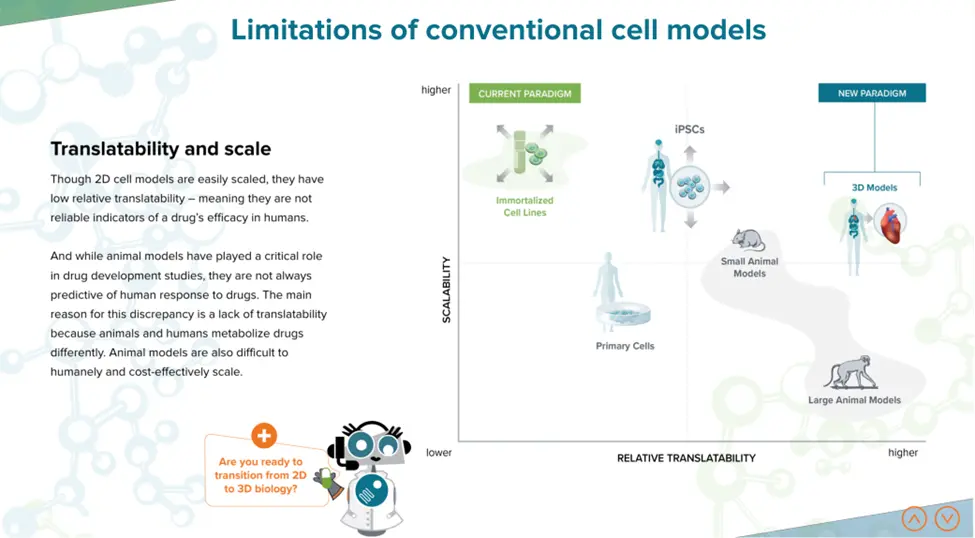
これに対処するため、創薬パラダイムでは、創薬を通じてヒトに関連するモデル系を活用し、臨床成功率を向上させ、動物モデルへの依存を減らしています。オルガノイドは、薬剤の結果を正確に予測することで、トランスレーショナルなギャップを減らしています。研究によると、前臨床試験で患者オルガノイド上で失敗した薬剤は、実際の患者でも失敗する可能性が高く、一方、高い成功率は患者の効果的な転帰につながります。
その可能性にもかかわらず、オルガノイドの培養には労力と時間がかかり、スケーラビリティに影響します。しかし、自動化技術やアッセイ準備の整ったオルガノイドは、拡張性を高め、その採用をより現実的なものにしています。
オルガノイドの規制強化

FDAは、研究におけるオルガノイドやその他の複雑なin vitroモデルの使用を支持する姿勢を強めています。これは、2022年に議会がFDA近代化法2.0を可決し、新薬が初めて動物実験以外の方法で承認されるようになったことからも明らかです。この転換により、創薬はより倫理的になり、より効果的で効率的なものになる可能性があります。
オルガノイド技術
臓器のミニチュア版であるオルガノイドは、そのユニークな機能によって医学研究に革命をもたらしています。例えば脳オルガノイドは、ヒトの脳の発達や神経疾患に関する貴重な洞察をもたらし、医薬品の試験や遺伝子変異の研究に理想的です。腸上皮を正確に再現した腸オルガノイドは、腸に関する細胞生物学、再生、疾患表現型の理解に不可欠です。腫瘍バイオマーカーを分析し、最も効果的な抗がん剤をスクリーニングすることで、個別化医療を可能にします。肺オルガノイドは気道の複雑な構造と機能を再現しており、呼吸器疾患における薬剤スクリーニングや疾患モデリングに最適です。
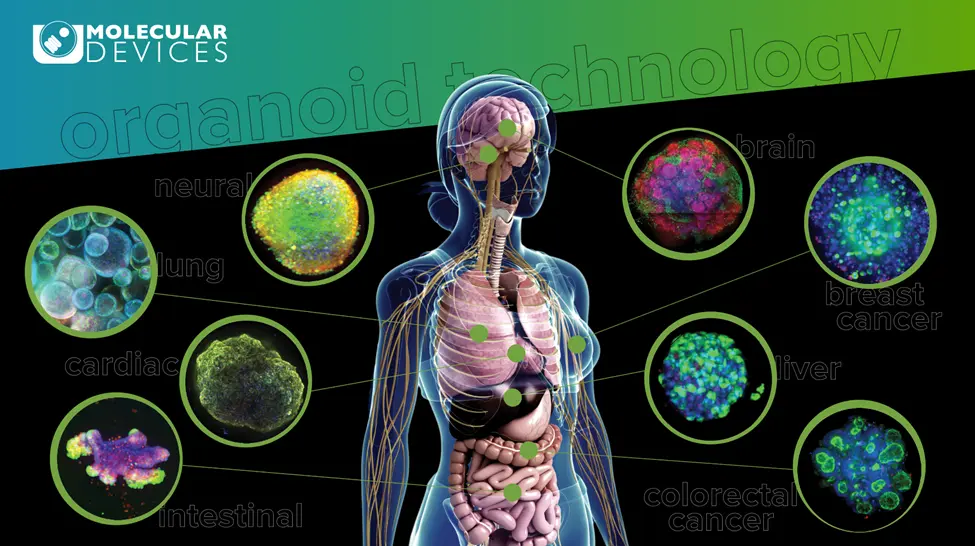
これらの多様なオルガノイドを組み合わせることで、医学研究と治療法開発における画期的な進歩への道が開かれます。
オルガノイドの3つの主要使用例
オルガノイドは体内の臓器に非常によく似ているため、ヒトの病気を研究したり、薬剤をスクリーニングしたり、潜在的な治療法をテストしたりするための正確な3D細胞モデルであることが証明されています。また、精密医療に特に有用なツールでもあります。例えば、患者由来のオルガノイドを特異性のある疾患患者から作製し、疾患の理解を深め、薬剤を開発し、個別化治療をカスタマイズするために使用することができます。

疾患モデル
疾患モデルは生物医学研究の礎であり、制御された環境で疾患の挙動を模倣するシステムを提供することで、その根本的なメカニズムを解明し、潜在的な治療法を検証します。
二次元細胞培養や動物のような従来のモデルには限界がありますが、オルガノイドはヒト組織の複雑さを再現することで、信頼できる代替手段を提供します。そのため、アルツハイマー病、心不全、がんなどの疾患の研究に理想的です。オルガノイドはまた、希少疾患研究を推進するためのより利用しやすいソリューションを提供し、世界中で4億人が罹患している7,000の希少疾患の治療法を発見する可能性があります。
薬物スクリーニング
ハイスループット・ドラッグスクリーニング(HTS)は、マルチウェルプレートによる数百万化合物ライブラリーの迅速なテストを可能にし、1990年代に革命をもたらしました。このアプローチは、膨大なライブラリーに含まれるすべての化合物をテストし、数個の活性のある化合物を見つけることを目的としていましたが、そのプロセスは煩雑で、しばしば臨床的に適切な結果を得ることができませんでした。
今日では、2Dモデルからオルガノイドのような高度な3Dバイオロジーモデルへの移行と自動化技術およびAI技術の組み合わせにより、HTSの精度と関連性が向上し、最も有望な薬剤候補をより迅速に特定することが可能になっています。
PDOs
患者由来オルガノイド(PDO)または腫瘍細胞は、個々の患者の腫瘍に由来するヒト関連モデルを提供することで、創薬研究や癌研究に革命をもたらしています。腫瘍の生検や手術サンプルから作製されたこれらの3D培養物は、元の腫瘍の分子特性を維持し、がん幹細胞のような性質を示します。そのため、患者特異的な薬物反応を理解し、腫瘍バイオマーカーを分析し、最も効果的な抗癌剤をスクリーニングする上で非常に貴重なものとなります。乳がんや大腸がんなどの困難ながんにおいて、PDOは、特に自動化、ハイコンテントイメージング、AIデータ解析によってサポートされた場合、精密医療やハイスループット創薬アプリケーションにおいて優れた可能性を示しています。
オルガノイドの課題
3Dバイオロジーの導入は、2D細胞モデルよりも予測可能性が高く、生物学的により適切なデータを提供するオルガノイドの有望性にもかかわらず、大きな障壁をもたらす可能性があります。しかし、これらの課題を理解することは、プロセスを合理化し、より安全で患者にとって必要な治療法をより早く提供するための解決策を見つけるためのワンステップです。

求められる抜本的イノベーション
創薬に革命を起こすには、オルガノイド技術にイノベーションを取り入れることが不可欠です。プロトコルを進化させ、自動化を活用し、AIの力を取り入れることで、精度を向上させ、コストを削減し、創薬のタイムラインを早めることができます。
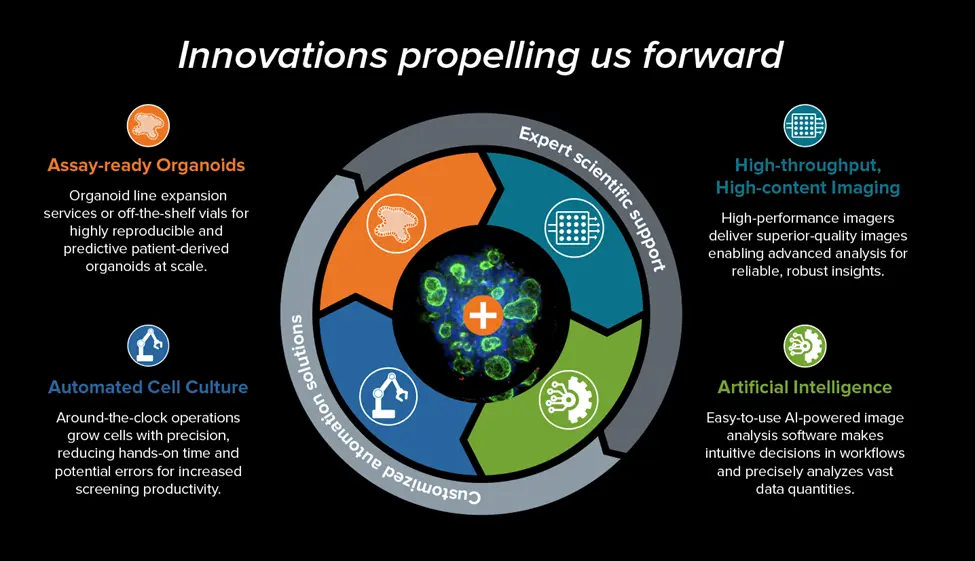
アッセイ対応オルガノイド
3D Ready™オルガノイドおよびオルガノイド拡大サービスを通じて、当社は特許取得済みバイオリアクターおよびバイオプロセス技術を用いて、高品質で信頼性の高いPDOをスケール生産しています。これには、キュレーションされた系統からのアッセイ・レディなオルガノイドと、特異性研究のニーズに合わせて特許取得済みオルガノイド系統を拡張する機能の両方が含まれ、様々な用途に一貫した高品質のヒト関連モデルを提供します。
ハイスループット、ハイコンテントイメージング
高性能イメージングは、正確なデータ解析と発見に必要な詳細で高解像度の画像を提供することで、科学研究において重要な役割を果たしています。ImageXpress®ハイコンテントイメージングシステムは、高画質、高速性、豊富なデータ量、分析精度を兼ね備えており、複雑な生物学のプロセスを鮮明に可視化することで、より深い洞察を得ることができます。
人工知能(AI)
IN Carta™画像解析ソフトウェアは、科学研究のための画像解析とワークフロー効率に革命をもたらす強力なAI/MLソフトウェアです。当社の自動細胞培養システムに統合され、一貫したワークフローの自動化、最適な細胞培養の供給、タイムリーな継代などの情報を最終的に画像から得ることで、意思決定を簡素化し、実験の精度を高めます。また、この解析機能は複雑な画像を解釈しやすい結果に形質転換し、深いデータサイエンスの専門知識を必要とすることなく、データの探索、表現型の変化の同定、新規の洞察の発見を容易に行うことができます。
細胞培養の自動化
CellXpress.ai™自動細胞培養システムは、複雑な給餌および継代スケジュールを管理するための機械学習を統合することにより、オルガノイド増殖の反復作業を軽減します。先進のハードウェアとソフトウェア技術を組み合わせることで、2Dおよび3D細胞培養プロセスを自動化・標準化し、オルガノイド研究のあらゆる段階で研究者をサポートし、iPS細胞、腫瘍細胞、成体幹細胞由来のオルガノイドのワークフローをガイドします。AIを搭載したソフトウェア、効率的なプロトコル開発、包括的なイベントロギングにより、信頼性と再現性の高い結果をスケールアップして提供します。
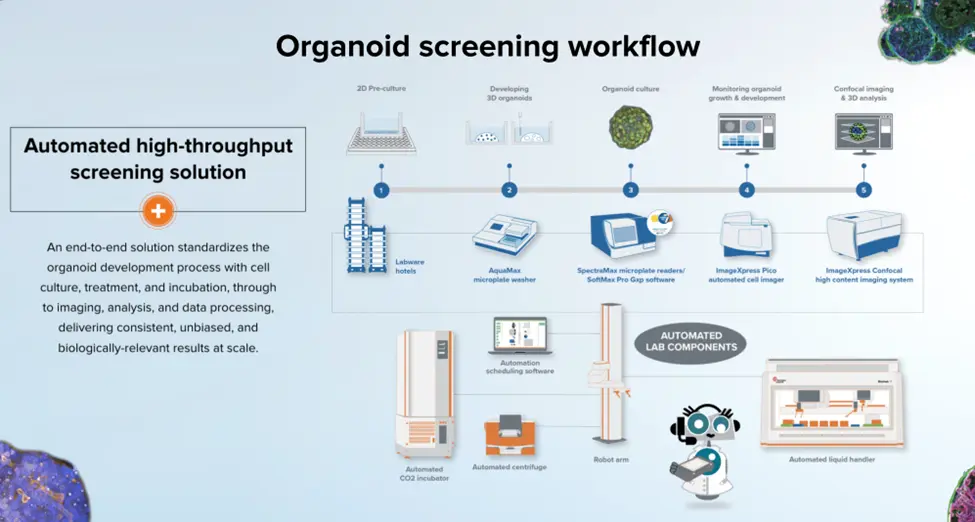
オルガノイドスクリーニングのワークフロー
高度な創薬のための効果的な自動エンドツーエンドワークフローの導入は、オルガノイド開発プロセスを標準化・合理化し、スループットと精度の両方を向上させる能力にかかっています。実績のあるハードウェアとソフトウェアソリューションをインテグリティすることで、自動ワークフローは、細胞の2D前培養からハイコンテント共焦点イメージング、AIを活用したデータ解析まで、すべてを促進することができます。
オルガノイド イノベーション センターへようこそ
オルガノイドイノベーションセンターは、複雑な3Dバイオロジーモデルで実施されるアッセイのサンプル前処理から報告までのパイプラインの各ステップに関連する課題に対処する完全統合型ソリューションを示しています。エンドツーエンドソリューションは、細胞培養、処理、インキュベーションからイメージング、解析、データ処理に至るまで、オルガノイド開発プロセスを標準化し、一貫性があり、偏りのない、生物学的関連性の高い結果をスケールアップして提供します。

2Dバイオロジーから3Dバイオロジーへの移行を模索するきっかけになりましたか?オルガノイドの課題に対する解決策を見つけるためですか?あるいは、すでに行っている研究の規模を拡大したいですか?
当社のエキスパートがお手伝いします。まずはお気軽にお問い合わせください。